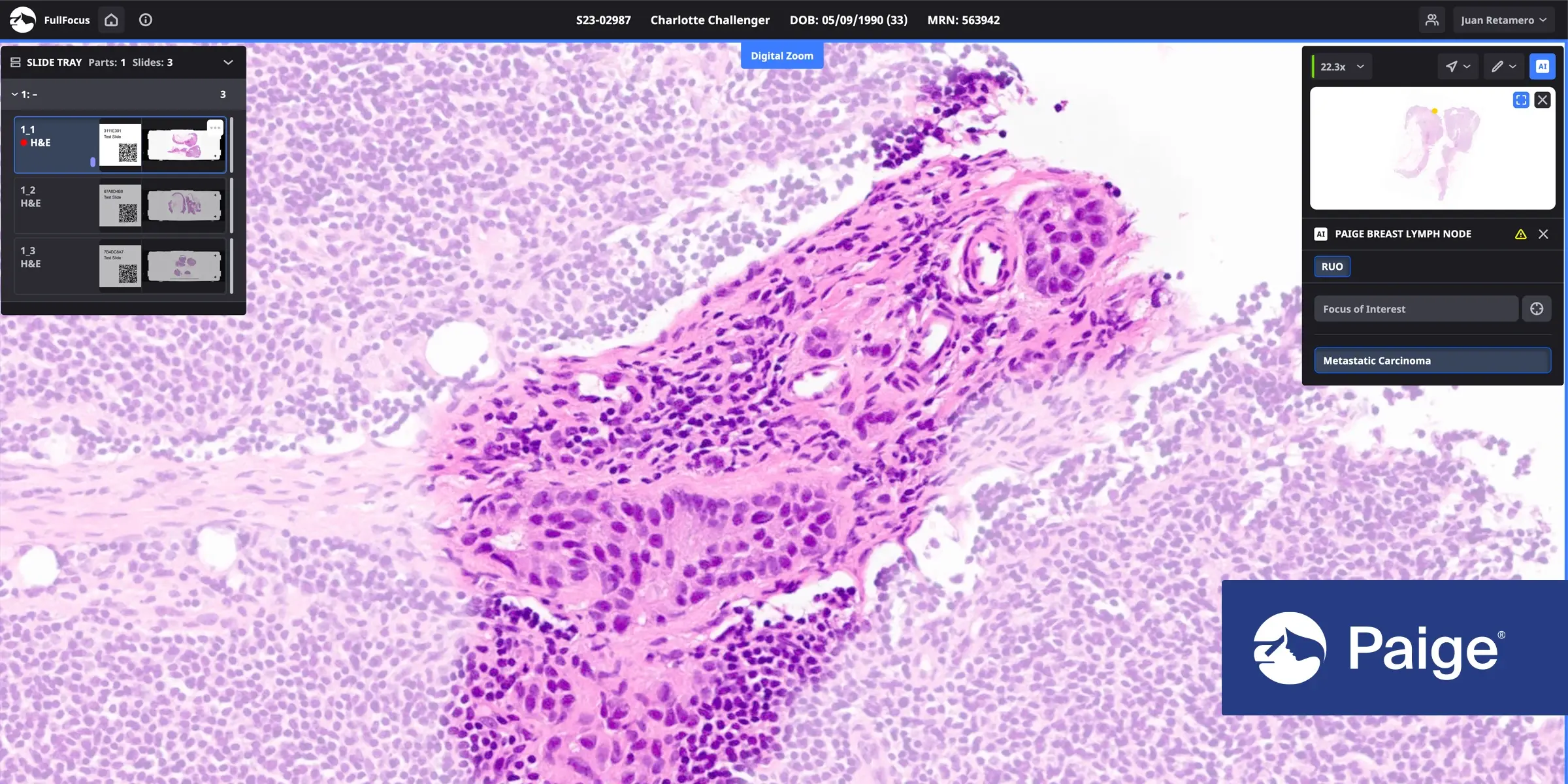
Paige Lymph Node est reconnu par la FDA comme un dispositif révolutionnaire pour aider les pathologistes à détecter les métastases du cancer du sein dans les tissus des ganglions lymphatiques.
NEW YORK–(FIL D’AFFAIRES)–Paige, leader mondial des solutions de pathologie numérique de bout en bout et des applications cliniques d’IA qui aident à diagnostiquer le cancer, a annoncé aujourd’hui que la Food and Drug Administration (FDA) des États-Unis a accordé la Breakthrough Device Designation au Paige Lymph Node1une application d’IA utilisée pour détecter les métastases du cancer du sein dans les tissus des ganglions lymphatiques. Paige Lymph Node est la première application d’IA de ce type à recevoir la désignation Breakthrough Device de la FDA.
La désignation par la FDA d’un dispositif révolutionnaire (Breakthrough Device Designation) est accordée aux technologies qui ont le potentiel de fournir un diagnostic ou un traitement plus efficace pour les maladies qui mettent la vie en danger ou qui sont irréversiblement débilitantes. Pour ces technologies, la mise à disposition en temps utile est dans le meilleur intérêt des patients parce qu’il n’existe pas d’alternative approuvée ou parce que la technologie offre des avantages significatifs par rapport aux alternatives approuvées existantes4.
« L’évaluation pathologique des ganglions lymphatiques chez les patientes atteintes d’un cancer du sein est d’une importance cruciale pour la prédiction du résultat et du traitement, mais le processus prend du temps et est sujet à des erreurs », a déclaré David S. Klimstra, M.D., fondateur et directeur médical de Paige. « Paige Lymph Node utilise la puissance de l’IA pour aider le pathologiste à identifier rapidement et avec précision les métastases ganglionnaires, même de petite taille, garantissant ainsi aux patientes atteintes d’un cancer du sein une prise en charge optimale de leur maladie. »
Paige Lymph Node est un logiciel de dispositif médical de diagnostic in vitro, dérivé d’un modèle d’apprentissage profond qui a été entraîné avec plus de 32 000 lames numérisées de ganglions lymphatiques à l’hématoxyline et à l’éosine (H&E). Le ganglion lymphatique de Paige détecte la présence de métastases du cancer du sein avec une sensibilité quasi parfaite3. Si le tissu du ganglion lymphatique est suspect de cancer, Paige Lymph Node mettra en évidence chaque zone préoccupante pour un examen plus approfondi par le pathologiste, ce qui rendra l’évaluation et le diagnostic plus faciles et plus efficaces.
« Nous sommes ravis de la décision de la FDA de reconnaître l’importance de l’IA dans la gestion de la maladie métastatique chez les patientes atteintes d’un cancer du sein », a déclaré Andy Moye, PhD, PDG de Paige. « L’algorithme Paige sur les ganglions lymphatiques permet aux pathologistes de gagner du temps et de disposer d’informations essentielles pour étayer leur diagnostic dans un contexte de demandes et de contraintes de ressources sans précédent ».
Paige a déjà obtenu la désignation de percée pour Paige Prostate Detect2, une application d’IA conçue pour faciliter l’identification des tissus cancéreux de la prostate, avant de devenir la première et la seule application de pathologie numérique autorisée par la FDA à ce jour. Paige FullFocus®2, une visionneuse d’images de lames entières, a également été approuvée par la FDA pour une utilisation dans le diagnostic primaire.
—
1AuxÉtats-Unis, le ganglion lymphatique de Paige est réservé à la recherche et ne doit pas être utilisé dans les procédures de diagnostic.
2 Aux États-Unis, le Paige Prostate Detect (DEN200080) a été approuvé pour une utilisation clinique avec le scanner ultra-rapide de Philips.
3Selonune étude clinique expérimentale menée par Paige, impliquant 3 pathologistes et les données de 148 patients.
4https://www.fda.gov/regulatory-information/search-fda-guidance-documents/breakthrough-devices-program