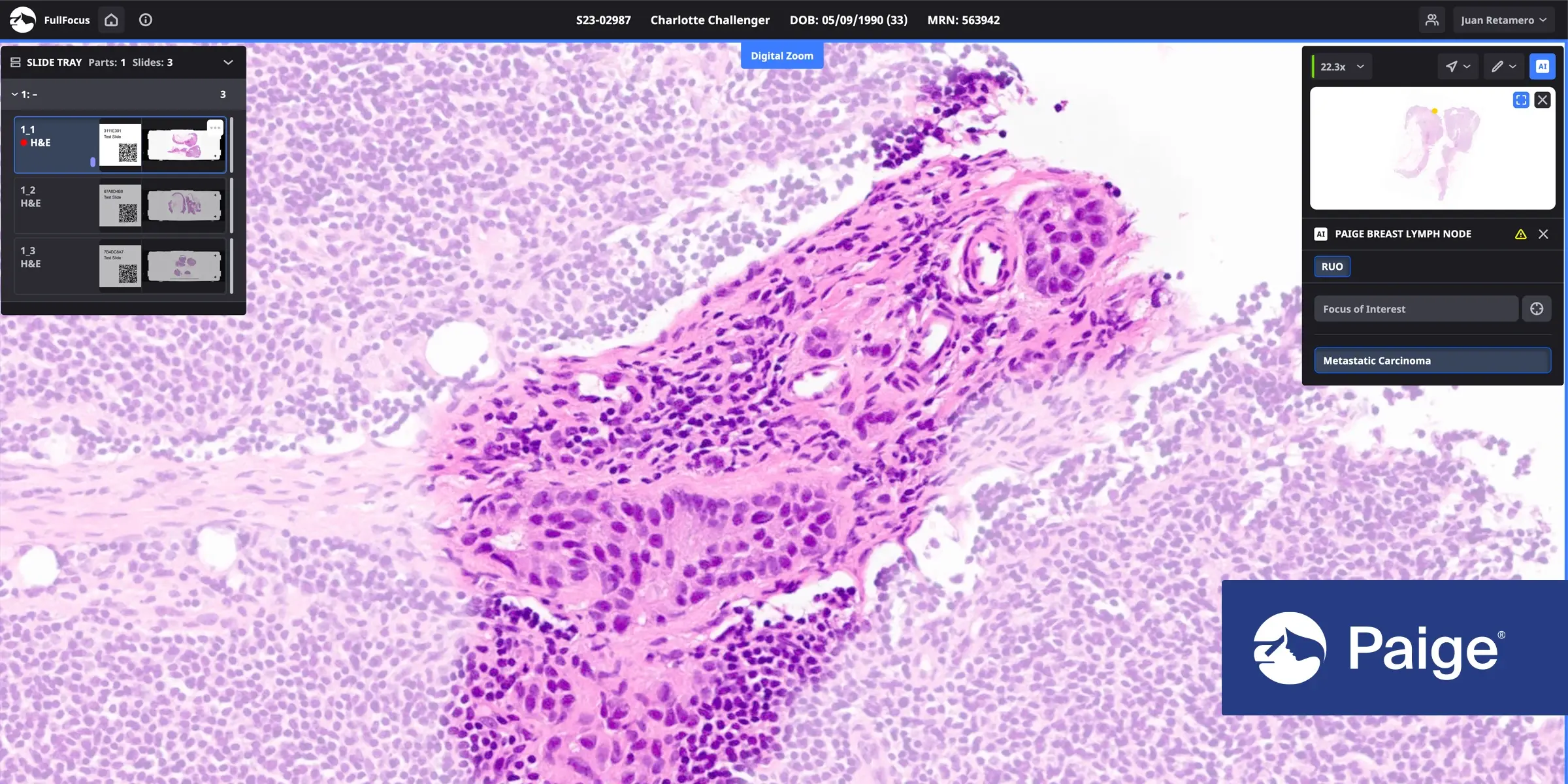
Paige Lymph Node ist von der FDA als bahnbrechendes Gerät anerkannt, das Pathologen bei der Erkennung von Brustkrebsmetastasen im Lymphknotengewebe unterstützt.
NEW YORK–(BUSINESS WIRE)–Paige, ein weltweit führender Anbieter von digitalen End-to-End-Pathologielösungen und klinischen KI-Anwendungen, die bei der Krebsdiagnose helfen, gab heute bekannt, dass die US-amerikanische Gesundheitsbehörde FDA (Food and Drug Administration) Paige Lymphknoten die Breakthrough Device Designation erteilt hat1, eine KI-Anwendung zur Erkennung von Brustkrebsmetastasen im Lymphknotengewebe. Paige Lymphknoten ist die erste KI-Anwendung ihrer Art, die von der FDA die Bezeichnung „Breakthrough Device Designation“ erhalten hat.
Die FDA erteilt die Bezeichnung „Breakthrough Device Designation“ für Technologien, die das Potenzial haben, eine wirksamere Diagnose oder Behandlung von lebensbedrohlichen oder irreversibel schwächenden Krankheiten zu ermöglichen. Bei diesen Technologien liegt die rechtzeitige Verfügbarkeit im besten Interesse der Patienten, weil es keine zugelassene Alternative gibt oder weil die Technologie erhebliche Vorteile gegenüber den bestehenden zugelassenen Alternativen bietet4.
„Die pathologische Beurteilung von Lymphknoten bei Brustkrebspatientinnen ist von entscheidender Bedeutung für die Vorhersage des Ergebnisses und der Behandlung, doch der Prozess ist zeitaufwändig und fehleranfällig“, sagte Dr. David S. Klimstra, Gründer und Chief Medical Officer bei Paige. „Paige Lymph Node nutzt die Leistungsfähigkeit der KI, um dem Pathologen dabei zu helfen, selbst kleine Lymphknotenmetastasen schnell und genau zu identifizieren und damit sicherzustellen, dass Brustkrebspatientinnen die optimale Behandlung ihrer Krankheit erhalten.“
Paige Lymph Node ist eine Software für In-vitro-Diagnostik, die auf einem Deep-Learning-Modell basiert, das mit über 32.000 digitalisierten Hämatoxylin- und Eosin-Objektträgern (H&E) von Lymphknoten trainiert wurde. Der Paige Lymphknoten erkennt das Vorhandensein von Brustkrebsmetastasen mit nahezu perfekter Empfindlichkeit3. Wenn das Lymphknotengewebe krebsverdächtig ist, hebt Paige Lymph Node jeden bedenklichen Bereich für die weitere Untersuchung durch den Pathologen hervor, so dass dieser leichter und effizienter zu einer Diagnose gelangen kann.
„Wir sind sehr erfreut über die Entscheidung der FDA, die Bedeutung der künstlichen Intelligenz bei der Behandlung von metastasierenden Erkrankungen bei Brustkrebspatientinnen anzuerkennen“, sagte Dr. Andy Moye, CEO von Paige. „Der Paige-Lymphknoten-Algorithmus spart Pathologen Zeit und liefert ihnen wichtige Informationen zur Unterstützung ihrer Diagnose in einer Zeit, in der die Anforderungen und die Ressourcen noch nie so hoch waren.“
Paige hatte zuvor den Status eines Durchbruchs für Paige Prostate Detect2 erlangt, eine KI-Anwendung, die bei der Identifizierung von krebsartigem Prostatagewebe helfen soll, bevor sie als erste und bisher einzige von der FDA zugelassene digitale Pathologieanwendung ausgezeichnet wurde. Paige FullFocus®2, ein Ganzbildbetrachter, wurde ebenfalls von der FDA für den Einsatz in der Primärdiagnostik zugelassen.
—
1 In denVereinigten Staaten ist der Paige-Lymphknoten nur für Forschungszwecke bestimmt und sollte nicht für diagnostische Verfahren verwendet werden.
2 In den Vereinigten Staaten ist Paige Prostate Detect (DEN200080) für die klinische Verwendung mit dem Philips Ultrafast Scanner zugelassen.
3Basierendauf einer von Paige durchgeführten klinischen Studie, an der 3 Pathologen beteiligt waren und Daten von 148 Patienten erhoben wurden.
4https://www.fda.gov/regulatory-information/search-fda-guidance-documents/breakthrough-devices-program